美國艾倫腦科學研究所揭示阿爾茨海默病的革命性多模態(tài)細胞圖譜
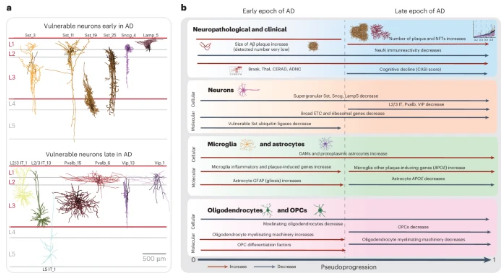
2024年10月14日�,美國艾倫腦科學研究所Ed S.Lein團隊在期刊《Nature Neuroscience》上發(fā)表了題為“Integrated multimodal cell atlas of Alzheimer’s disease”的研究論文。團隊使用定量神經病理學���,將供體置于疾病假性進展評分中��。假性進展分析揭示了兩個疾病階段:病理學緩慢增加的早期階段�,存在炎性小膠質細胞���、反應性星形膠質細胞��、生長抑素抑制神經元丟失��,以及少突膠質細胞前體細胞的髓鞘再生反應�;病理學呈指數級增加的后期��,興奮性神經元���、Pvalb和Vip抑制性神經元亞型的丟失��。
關于阿爾茨海默病
阿爾茨海默?��。ˋD)的特征是標志性病理肽沉積和神經退行性變,這些肽在部分重疊的神經解剖軸和顳軸上進展�。通常認為���,這個過程遵循從大腦皮層開始出現β淀粉樣蛋白(Aβ)斑塊的刻板印象,以及始于腦干和邊緣系統(tǒng)的過度磷酸化Tau (pTau)聚集(神經原纖維纏結 (NFT))�。
由BRAIN Initiative細胞普查網絡(BICCN)和BRAIN Initiative Cell Atlas Network(BICAN)催化的新工作在實驗和定量分析方面建立了較佳實踐,以利用單細胞基因組學�、空間轉錄組學和補丁測序(patch-seq)方法,來表征細胞特性并建立腦細胞類型的知識庫����。BICCN和BICAN正在繪制第一個小鼠和人腦的全腦細胞圖譜。
目前的研究集中在顳中回(MTG)����,這是一個涉及語言、語義記憶處理和高階視覺處理的領域�。許多研究證明,MTG是衰老或臨床前AD相關的內側顳葉pTau與AD更高級階段之間的過渡區(qū)��,新皮層pTau延伸到大腦中�����,與癡呆密切相關����。這種將跨研究數據整合到公共參考的策略具有高度可擴展性�����,并為AD社區(qū)提供了一個統(tǒng)一的框架。研究數據可在SEA-AD的網站(https://portal.brain-map.org/explore/seattle-alzheimers-disease)上免費獲得���。
受AD影響的MTG細胞����,主要定位于表層���,可以分為兩個時期:早期和晚期���。
OPC引起的少突膠質細胞丟失和髓鞘再生
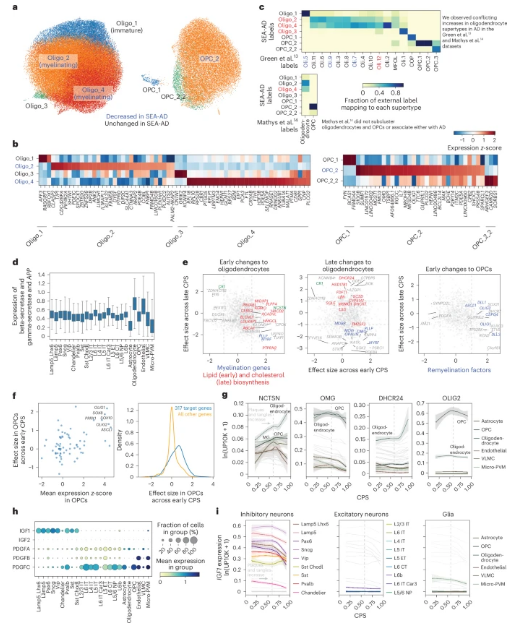
少突膠質細胞功能障礙和髓鞘分解,可能是AD的早期事件�����。在少突膠質細胞中���,兩種超型(Oligo_2和Oligo_4)在MTG和A9的早期都很脆弱�。在BRAIN Initiative參考數據集的整個皮層柱中����,都可以找到這兩種超類型��。CNP在兩者中均有表達(盡管Oligo_4中更高)����,表明它們是髓鞘少突膠質細胞���。團隊還觀察到一種OPC超型(OPC_2)的晚期減少�,該超型(OPC超型)在皮質層2至6中發(fā)現�����。與公開可用的數據集相比�����,SEA-AD少突膠質細胞和OPC���,在很大程度上與參考文獻中描述的細粒度類型一致���。大多數超類型具有一對一或一對多關系。
團隊檢查了對OPC分化為少突膠質細胞很重要的兩種信號通路的表達:胰島素樣生長因子(IGF)和血小板衍生生長因子(PDGF)���。雖然PDGF基因的表達跨越多個細胞亞類�����,但IGF的表達僅限于抑制性中間神經元和一小部分小膠質細胞�����。CPS中后期��,IGF1表達在幾個抑制性中間神經元群中降低���,表明這些抑制性群體可能是IGF1的主要來源和髓鞘形成變化的驅動因素。
在公開可用的數據集中�,OPC中髓鞘再生程序的少突膠質細胞早期丟失。
總結
1. AD綜合圖譜的構建:美國艾倫腦科學研究所在大腦的中顳回(MTG)區(qū)域描述了阿爾茨海默?。ˋD)的綜合圖譜,該區(qū)域是AD病理學的過渡區(qū)域�,也是細胞類型表型聚合知識較多的區(qū)域。
2. AD進展的兩個主要時期:早期階段病理水平較低���,認知不受影響�����,但神經元丟失和早期淀粉樣蛋白病理出現�;晚期階段,AD病理��、神經元丟失和認知障礙顯著增加���。
3. 神經元和非神經元細胞的變化:在AD的早期和晚期�����,不同類型的神經元和非神經元細胞表現出不同的變化�����,包括特定類型的興奮性神經元和抑制性神經元的丟失����。
4. AD病理學的生物學結果:研究結果表明��,嚴重受影響的供體表現出廣泛的細胞功能障礙����,這可能是AD病理學和隨后的認知能力下降的生物學結果。
5. 研究的臨床意義:該研究提供了對AD細胞和分子事件的詳細理解,有助于定義受影響細胞的具體類型��、位置和疾病進展中的時間點����,為未來的治療策略提供了潛在的靶點。
聲明:本文版權歸原作者所有���,轉載文章僅為傳播更多信息���,如作者信息標記有誤,或侵犯您的版權���,請聯(lián)系我們,我們將在及時修改或刪除內容�,聯(lián)系郵箱:marketing@360worldcare.com