FDA批準(zhǔn)Opdivo用于晚期食管鱗狀細(xì)胞癌
6月10日�����,BMS宣布FDA批準(zhǔn)其Opdivo新適應(yīng)癥���,用于治療無法切除的晚期��、復(fù)發(fā)或轉(zhuǎn)移性食管鱗狀細(xì)胞癌(ESCC)患者�����,這些患者先前接受過氟尿嘧啶和鉑類藥物的治療����。這是一個(gè)獲批用于治療該類患者人群的免疫療法,無論P(yáng)D-L1狀態(tài)如何�。

此次批準(zhǔn)是基于III期ATTRACTION-3研究結(jié)果,該研究顯示�,Opdivo治療組(n=210)較紫杉烷類化療組(n=209)生存期獲得了延長(HR 0.77;95%CI: 0.62-0.96; p=0.0189),Opdivo組的中位OS為10.9個(gè)�,紫杉烷類化療組為8.4個(gè)月。
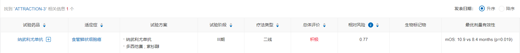
來源:NextPharma
據(jù)估計(jì)���,美國2020年預(yù)計(jì)新增確診食管癌患者18440例�����,死亡人數(shù)約16170例�����。其中���,大約不到30%的患者為食管鱗狀細(xì)胞癌�。大約25%的患者確診時(shí)已是晚期����,通常難以治療。
聲明:本文版權(quán)歸原作者所有��,轉(zhuǎn)載文章僅為傳播更多信息�����,如作者信息標(biāo)記有誤����,或侵犯您的版權(quán),請(qǐng)聯(lián)系我們��,我們將在及時(shí)修改或刪除內(nèi)容���,聯(lián)系郵箱:marketing@360worldcare.com

