在生命運轉(zhuǎn)過程中����,人體細胞持續(xù)不斷地進行著分裂�,每次都需要高精度地復(fù)制30億個DNA堿基����,以確保細胞的存活。但是研究人員發(fā)現(xiàn)����,在癌癥中卻并非如此。
6月5日,由悉尼加文醫(yī)學(xué)研究所的David Thomas教授所領(lǐng)導(dǎo)的研究小組在Science雜志上發(fā)表了一項突破性研究����,研究結(jié)果顯示,包括黑色素瘤�����、胰腺癌����、肉瘤和乳腺癌在內(nèi)的多種癌癥,在接受治療后會啟動易錯的DNA復(fù)制路徑產(chǎn)生大量的復(fù)制錯誤來形成耐藥性����,從而適應(yīng)癌癥治療。

圖片來源:Science
逃脫癌癥治療
癌癥治療的耐藥性每年都影響著成千上萬的癌癥患者��,即使是先進的治療方法��,也會帶來身體難以承受的健康結(jié)局���。
研究者們早就知道癌細胞會積累遺傳變異��,從而使其有可能逃避治療��。但逃避如何發(fā)生以及逃避過程是否可以被靶向以改善癌癥治療卻一直難以破解���。
靶向療法通過干擾腫瘤生長所需的一些分子來阻止癌細胞的生長�����,是很多種癌癥的常見治療方法�����。在本項研究中�,研究人員通過對癌癥患者接受靶向癌癥治療之前和之后的活檢樣進行分析來探尋產(chǎn)生癌癥治療耐藥性可能的驅(qū)動因素��。
結(jié)果令人驚訝��。在接受靶向療法的患者中���,即使這些治療并未直接損傷DNA,但其癌細胞顯示出的DNA損傷水平要比治療前的樣本高得多�����。
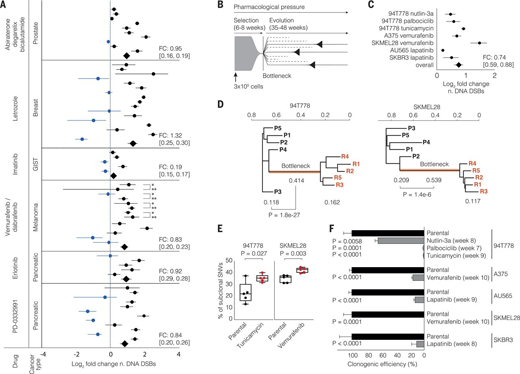
靶向抗癌療法的選擇導(dǎo)致了遺傳多樣性(圖片來源:Science)
論文一作者Arcadi Cipponi博士說:“我們的試驗表明�,接受靶向療法的癌細胞經(jīng)歷了一種稱為應(yīng)激誘導(dǎo)突變(stress-induced mutagenesis)的過程�,它們的隨機基因變異的發(fā)生率要比未接受抗癌藥物的癌細胞高得多�。這是一個古老的過程,細菌遇到壓力時也會使用相同的過程來進化��?����!?/span>
癌癥耐藥性的兩步走策略
為了研究人類癌細胞應(yīng)激誘變背后的機制����,研究人員進行了大規(guī)模篩選來沉默癌細胞中的每個基因,以確定導(dǎo)致癌細胞耐藥性的特定通路�����。
當編碼MTOR(一種壓力感受器蛋白)的基因被沉默時����,研究人員發(fā)現(xiàn),在開展抗癌治療的情況下����,癌細胞停止了生長,但反常地加速了進化���。
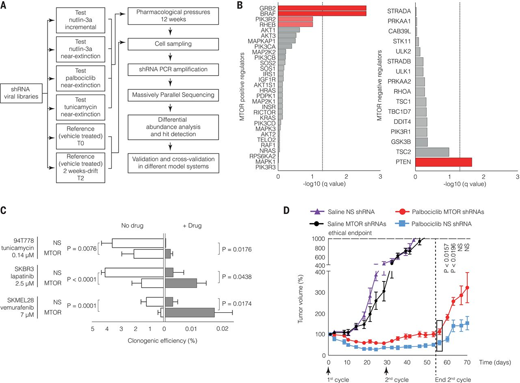
全基因組RNAi篩選確定MTOR是癌癥中常見的進化調(diào)控因子(圖片來源:Science)
“MTOR可以在受環(huán)境脅迫時向正常細胞傳達停止生長的信息��。但是我們發(fā)現(xiàn)���,在進行癌癥治療的情況下���,MTOR信號使癌細胞能夠改變DNA修復(fù)和復(fù)制相關(guān)基因的表達。例如�,從表達DNA復(fù)制高保真聚合酶轉(zhuǎn)變?yōu)橐族e的聚合酶。這導(dǎo)致了更多的遺傳變異�,加劇了對治療的耐藥性?���!盋ipponi博士說道。
這種向低保真DNA修復(fù)和復(fù)制的轉(zhuǎn)變是暫時的�����,一旦癌細胞獲得了對癌癥治療的耐藥性����,就會重新激活高保真途徑�����。
“某些化療和放療所導(dǎo)致的基因組不穩(wěn)定性本身可能對細胞有害。但癌細胞一旦對治療產(chǎn)生耐藥性�����,它們便會轉(zhuǎn)換回高保真DNA聚合酶途徑以確保已對治療進化出耐藥性的細胞能夠生存����。” Cipponi博士解釋說�。
癌癥治療的新方法
研究人員認為將常規(guī)的靶向癌癥療法與靶向DNA修復(fù)機制的藥物相結(jié)合,可能會更為有效�。
為了驗證這一理論,研究人員在胰腺癌小鼠模型中測試了一種藥物組合:CDK4/6抑制劑哌柏西利(這類藥物可恢復(fù)細胞周期控制�,阻斷腫瘤細胞增殖)+PARP抑制劑魯卡帕尼(一種可選擇性靶向DNA修復(fù)受損細胞的藥物)。結(jié)果表明與單獨使用哌柏西利相比����,哌柏西利與魯卡帕尼聯(lián)合使用可以在30天內(nèi)將癌癥生長降低近60%。
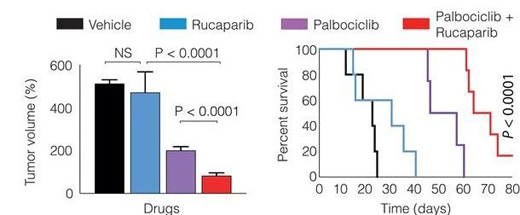
聯(lián)合療法增強了抗腫瘤作用(圖片來源:Science)
Thomas教授認為這些發(fā)現(xiàn)開辟了新的潛在癌癥治療策略��,對于癌癥中的應(yīng)激誘導(dǎo)突變具有預(yù)防作用�,或者在已產(chǎn)生耐藥性的癌癥中更為有效。
相關(guān)論文:
[1] Arcadi Cipponi, David L. Goode, Justin Bedo, et al. MTOR signaling orchestrates stress-induced mutagenesis, facilitating adaptive evolution in cancer. Science (2020)
參考資料:
1# Revealed: How cancer develops resistance to treatment(來源:Medical press)
聲明:本文版權(quán)歸原作者所有����,轉(zhuǎn)載文章僅為傳播更多信息����,如作者信息標記有誤��,或侵犯您的版權(quán)�����,請聯(lián)系我們�����,我們將在及時修改或刪除內(nèi)容����,聯(lián)系郵箱:marketing@360worldcare.com



